Що такеповерхневий натяг води?
Поверхневий натягце тенденція поверхонь спокою рідини стискатися до мінімально можливої площі поверхні. Поверхневий натяг дозволяє об’єктам із вищою щільністю, ніж вода, таким як леза для гоління та комахи (наприклад, водоплавці) плавати на поверхні води, не занурюючись навіть частково.
На межі розділу рідина-повітря поверхневий натяг є результатом більшого притягання молекул рідини одна до одної (через когезію), ніж до молекул у повітрі (через адгезію).
У грі є два основні механізми. Один — це внутрішня сила, що діє на поверхневі молекули, що змушує рідину стискатися. По-друге, це тангенціальна сила, паралельна поверхні рідини. ЦетангенціальнийСила зазвичай називається поверхневим натягом. Суттєвий ефект полягає в тому, що рідина поводиться так, ніби її поверхня покрита розтягнутою еластичною мембраною. Але ця аналогія не повинна бути надто далекою, оскільки напруга в еластичній мембрані залежить від величини деформації мембрани, тоді як поверхневий натяг є невід’ємною властивістю рідини.–повітря аборідинно-паровийінтерфейс.
Через відносно сильне притягання молекул води одна до одної через мережу водневих зв’язків вода має вищий поверхневий натяг (72,8 міліньютон (мН) на метр при 20 градусах), ніж більшість інших рідин. Важливим фактором явища капілярності є поверхневий натяг.
Чому мило порушує поверхневий натяг води?
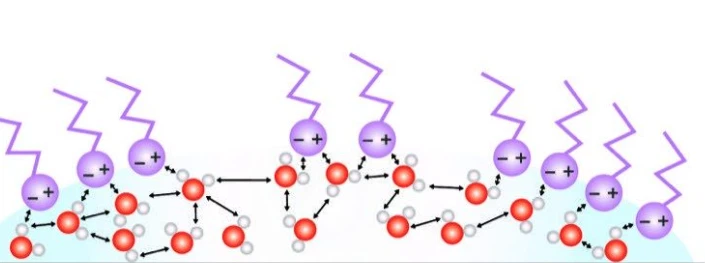
Мило порушує поверхневий натяг води завдяки своїй молекулярній структурі, яка містить як гідрофобні (водовідштовхувальні), так і гідрофільні (притягуючі воду) кінці. Молекули води на поверхні створюють «шкіру» завдяки силам когезії між ними, що призводить до високого поверхневого натягу.
Коли мило додається у воду, гідрофобні кінці молекул мила відштовхуються водою та просуваються на поверхню, тоді як гідрофільні кінці залишаються у воді. Це порушує когезійні сили між молекулами води на поверхні, зменшуючи поверхневий натяг. У результаті вода стає менш зв’язною та легше розтікається, дозволяючи їй краще змочувати поверхні.





